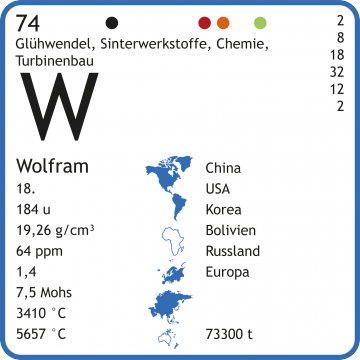
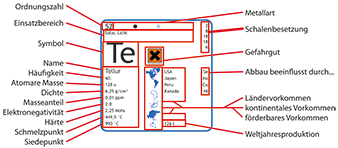
Tagesaktueller Wolfram-Preis
Wolfram-Chemie » Verbindungen
Wolfram bildet mehrere Oxide. Zwischen dem Anfangsglied:
- Wolfram(VI)-oxid WO3 – zitronengelb und dem Endglied
- Wolfram(IV)-oxid WO2 – braun gibt es noch folgende intermediäre Oxide:
- W10O29 blauviolett, Homogenitätsbereich WO2,92-WO2,88
- W4O11 rotviolett, Homogenitätsbereich WO2,76-WO2,73
- W18O49, WO2,72, rotviolettes Kristallpulver. Halbleiter. Dichte 7,72 g/cm3, Kristallstruktur: deformierter DO6-Typ, monoklin, Raumgruppe P2/m (Raumgruppen-Nr. 10), Gitterparameter: a = 1832 pm, b = 379 pm, c = 1404 pm, β = 115,2°.
- W20O50, WO2,50
Sonstige Verbindungen
- Natriumwolframat Na2WO4
- Zirkoniumwolframat ZrW2O8 zeigt beim Erwärmen eine Anomalie.
- Wolframoxidhydroxide bestimmter Zusammensetzung und mit Oxidationszahlen zwischen 5 und 6 haben eine blaue Farbe. Sie werden als Wolframblau bezeichnet und entsprechen in vielfacher Hinsicht dem Molybdänblau. Wolframblau dient als Nachweis von Wolframaten, aus denen es durch Reduktion entsteht.[47]
- Wolframbronzen MxWO3; M=Alkali-, Erdalkalimetall, Lanthanoid, ca. 0,3 < x < 0,9 besitzen elektrische Leitfähigkeit und sind intensiv und je nach Metallgehalt unterschiedlich gefärbt.
- Calciumwolframat CaWO4 ist als Mineral unter dem Namen Scheelit bekannt.
- Wolframcarbid WC ist eine extrem harte metallähnliche Verbindung. Daneben gibt es noch Diwolframcarbid W2C.
- Wolframhexafluorid WF6
- Bleiwolframat PbWO4
- Wolframdisulfid WS2 Einsatz als Trockenschmiermittel (Ähnlich MoS2)
Verwendung der Verbindungen
Wolframcarbid wird als Neutronenreflektor bei Kernwaffen eingesetzt, um die kritische Masse herabzusetzen. Wolframcarbide (Hartmetall) werden aufgrund ihrer hohen Härte in der Materialbearbeitung verwendet.
Wolframate werden zur Imprägnierung von Stoffen verwendet, um diese schwer entflammbar zu machen.
Wolframhaltige Farben werden in der Malerei sowie in der Keramik- und Porzellanindustrie verwendet.
Bleiwolframat wird als moderner Szintillator in der Teilchenphysik verwendet.

+49 89 744 88 88 88